О воде |
Жесткая вода
Все - жители городских квартир, владельцы коттеджей и загородных домов беспокоятся о качестве воды, которую они пьют и используют для бытовых нужд.
Одной из самых распространенных проблем при водоподготовке является повышенная жесткость воды, которая обусловлена наличием растворенных в ней большого количества ионов кальция.
Жесткостью воды называется сумма растворенных в воде ионов кальция Са2+ и магния Mg2+.
Первоначально термин «жесткая вода» применялся к воде, стирка в которой была затруднена.
Основным источником попадания в воду солей магния и кальция являются размываемые природными водами залежи известняков, гипса и доломитов..
В маломинерализованных водах больше всего ионов кальция.
С увеличением степени минерализации содержание ионов кальция быстро падает и редко превышает 1 г/л. Содержание же ионов магния в минерализованных водах может достигать нескольких граммов, а в соленых водах нескольких десятков граммов.
Ионы кальция и магния не приносят особого вреда живым организмам, однако наличие их в воде в большом количестве нежелательно, поскольку такая вода непригодна для хозяйственных нужд.
В жесткой воде увеличивается расход мыла и порошка при стирке белья, медленно разваривается мясо и овощи, снижается моторика желудка. Жесткая вода непригодна для систем водоснабжения и питания водонагревательной техники.
Жесткость измеряется в миллиграммах эквивалент на литр (мг-экв/л). Промышленные стандарты допустимого значения жесткости зависят от типа используемого оборудования. Обычно, считается жесткой вода с жесткостью 1 мг-экв/л и более.
|
Классификация воды по жесткости |
|||
|
Единицы измерения жесткости воды |
Грейн на галлон GPG |
Миллиграмм на литр, мг/л |
Миллиграмм-эквивалент на литр, мг-экв/л |
|
Мягкая |
< 1,0 gpg |
< 17,1 |
< 0,35 мг-экв/л |
|
Жестковатая |
1,0 - 3,5 gpg |
17,1 - 60 мг/л |
0,35 - 1,2 мг-экв/л |
|
Средней жесткости |
3,5 - 7,0 gpg |
60 - 120 мг/л |
1,2 - 2,4мг-экв/л |
|
Жесткая |
7,0 - 10,5 gpg |
120 - 180 мг/л |
2,4 - 3,6 мг-экв/л |
|
Очень жесткая |
> 10,5 gpg |
> 180 мг/л |
> 3,6 мг-экв/л |
Чтобы снизить жесткость, воду смягчают, используя специальный фильтр – умягчитель воды (ионообменный фильтр или смягчитель воды).
Как работает система умягчения?
Жесткая вода, поступая в умягчитель, проходит через слой ионообменной смолы засыпанной в фильтрующий резервуар и освобождается от солей жёсткости. Происходит ионный обмен: ионы кальция и магния, определяющие жёсткость воды, замещаются на ионы натрия, которыми насыщена смола. При истощении смолы, автоматический управляющий клапан переводит фильтр в режим регенерации и смола восстанавливается водным раствором высокоочищенной поваренной соли (NaCl), автоматически подающимся из бака солерастворителя. Происходит обратный процесс замещения накопленных ионов жёсткости на ионы натрия из солевого раствора. И умягчитель снова готов к работе! Все эти процессы происходят автоматически и единственное, что от Вас потребуется это раз в месяц засыпать таблетированную соль в бак солерастворитель и конечно же очередной раз полюбоваться на высокотехнологичное оборудование. Таблетированную соль для умягчителей продают практически все фирмы, специализирующиеся на водоочистке.
Почему вода жесткая?
Почему в воде из одного источника мыло хорошо мылится, а в воде из другого плохо? Говорят, плохо мылится потому, что жесткая вода. А что в ней такого жесткого? Давайте разберемся. Помните, в школе на уроке географии вам показывали примерно такую картинку? Она называется - круговорот воды в природе.
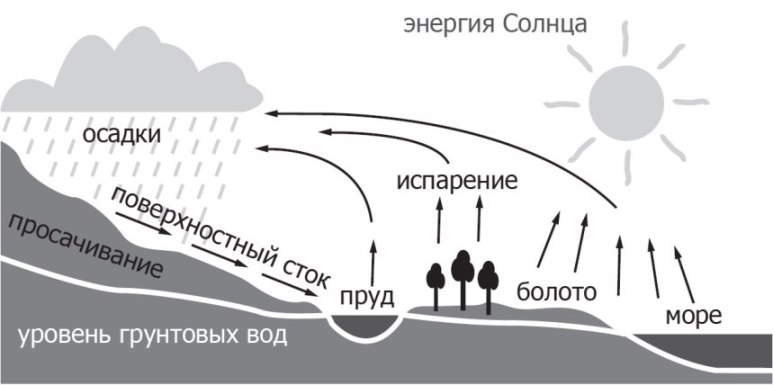
Под действием солнечного тепла вода испаряется с поверхности водоемов. Водяной пар поднимается в атмосферу, где из него образуются облака. Воздушные течения переносят облака на большие расстояния. Водяные пары конденсируются, образуются капельки воды, происходит выпадение осадков.
При этом влага впитывает и растворяет атмосферные газы, в основном углекислый газ, образуется раствор углекислоты. Поэтому дождевая вода немного кислая. А над промышленными районами дождевая вода еще более кислая, потому что там содержание углекислоты в воздухе выше, плюс в воздухе часто содержатся сернистые газы – образуется серная кислота.
Стекая по склонам, кислая дождевая вода растворяет соли кальция и магния, из которых состоят мягкие горные породы. Воду с высоким содержанием этих солей называют жесткой.
Различают временную жесткость воды и постоянную. Временная жесткость воды образуется за счет присутствия в воде карбонатов и гидрокарбонатов кальция и магния. Эти соли растворимы в воде, и они будут растворены в ней до тех пор, пока изменение давления или температуры не сделает раствор перенасыщенным. Тогда произойдет выпадение солей с образованием твердой корки накипи на нагретых или на неровных поверхностях, таких как трубы, теплообменники и нагревательные элементы. Постоянная жесткость обусловлена в основном присутствием в воде сульфатов кальция и магния. Эти соли не так чувствительны к изменениям давления и температуры, однако если вода будет испарена, они также образуют твердую корку накипи.






















